研究背景介绍
高危型人乳头瘤病毒(HR-HPV)相关疾病可治疗,但患者预后高度依赖于早期诊疗。便捷筛查技术的缺乏是全球HPV癌症发病率上升的关键因素,尤其在宫颈癌中,每年新增病例超过60万,80%发生在低收入和中等收入国家(LMICs)。HR-HPV持续感染导致宫颈癌,并可能引发肛门癌和头颈癌,严重威胁女性健康。HPV-16和HPV-18基因型在宫颈癌及其前期病变中占70%,早期诊断与干预对于提高生存率至关重要。然而,当前PCR相关筛查方法设备复杂、耗时长,在资源有限地区难以普及,导致宫颈癌及相关癌症死亡率居高不下。开发经济高效、快速准确且便于携带的HR-HPV分型检测方法,对于提升LMICs宫颈癌防控尤为关键,不仅补充现有筛查手段,也是实现全球卫生公平的重要一步。
为了解决这一难题,2025年3月31日,Advanced Science在线发表杂志raybet官网刘笔锋教授课题组题为“Deep Learning-Enhanced Hand-Driven Microfluidic Chip for Multiplexed Nucleic Acid Detection Based on RPA/CRISPR”的研究论文。东北大学与华科大联培徐涛博士、RAYBET雷竞技章英博士、李顺基博士为论文的共同第一作者。RAYBET雷竞技刘笔锋教授、陈鹏副教授与东北大学医学与生物信息工程学院田野特聘研究员为论文通讯作者。

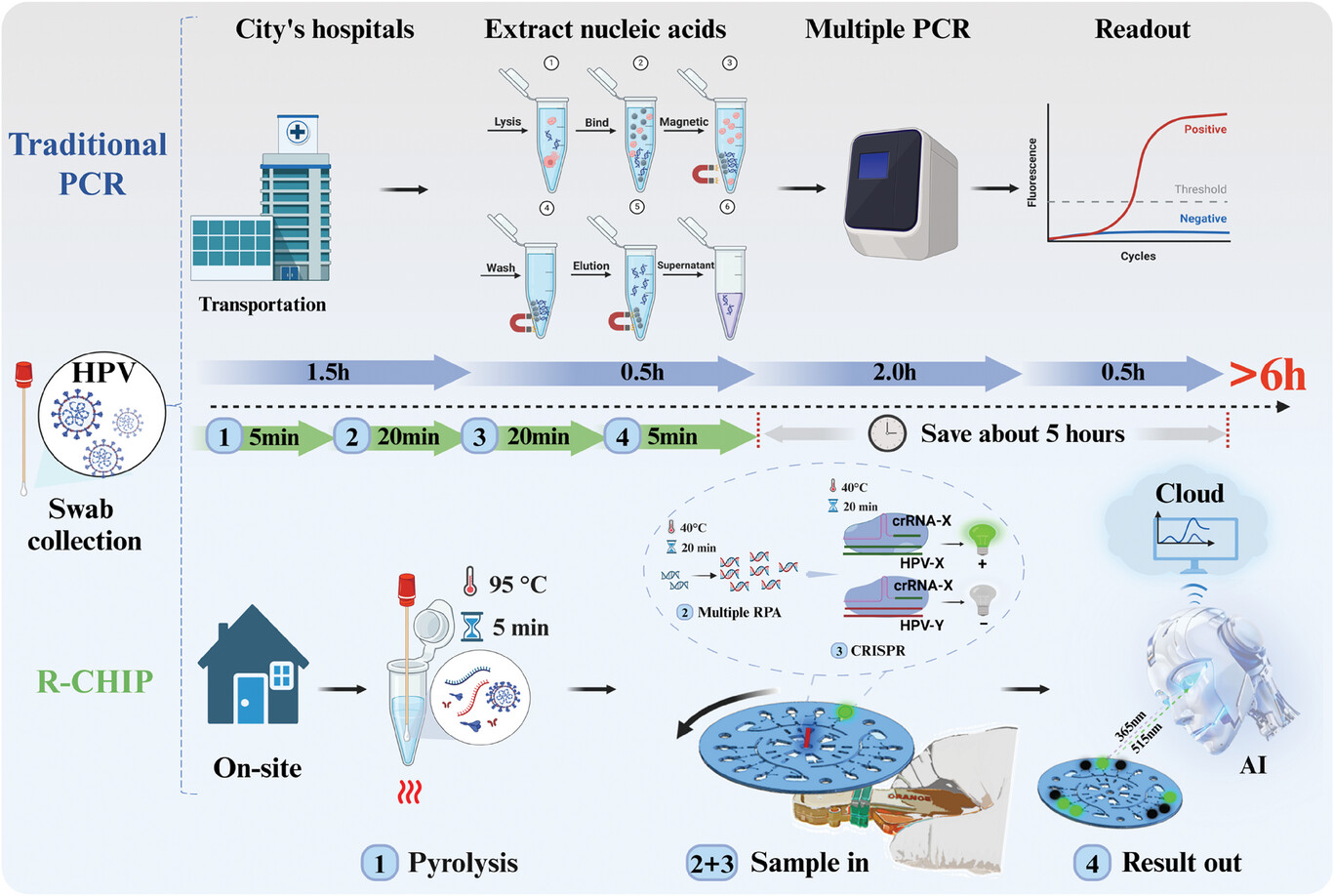
R-CHIP 微流控芯片筛查 HR-HPV 的流程图。R-CHIP 筛选过程包括样品热裂解、RPA 扩增和 CRISPR 切割检测。传统的 PCR 检测通常需要 6 个多小时才能报告结果(上图)。相比之下,R-CHIP 可以在 1 小时内提供结果(下图)。
该研究创新性地研发了一种基于手驱离心微流控芯片技术的智能化即时检测系统,通过整合重组酶聚合酶扩增(RPA)、CRISPR检测技术和深度学习图像识别技术,实现了多种HR-HPV的便携式、超灵敏及智能化检测。具体来说,研究团队首先利用离心力、毛细力与压力差之间的动态平衡,设计了手驱式离心微流控芯片。仅需单一的手动旋转操作即可完成核酸样本的扩增、预处理、试剂定量顺序释放、混合孵育及荧光检测等步骤,无需外部泵送系统。这种方法不仅避免了现行RPA/CRISPR“两步法”中反复开盖和液体转移引起的气溶胶污染问题,还解决了“一步法”中存在的特异性、稳定性、反应速率和灵敏度方面的限制。手驱式离心微流控芯片摆脱了对复杂机械控制和外部泵送系统的依赖,经过简单培训后普通人员即可操作,并能与家用加热设备及小型仪器兼容。整个检测过程在1小时内完成,极大地提升了HPV筛查的便捷性和可及性。
在此基础上,该研究进一步针对高危型人乳头瘤病毒HPV-16和HPV-18,设计并构建了多重RPA-CRISPR检测体系。通过对比常规的RPA-Exo荧光探针检测系统及传统的RPA凝胶电泳方法,验证了RPA-CRISPR技术的优势。研究发现,单独使用多重RPA扩增存在较高的非特异性背景信号问题,而采用RPA-CRISPR联合检测技术有效解决了这一问题,并显著提升了检测灵敏度(灵敏度低至10-18 M)。将RPA-CRISPR检测体系整合入R-CHIP微流控芯片后,芯片内外的检测结果显示出良好的灵敏度和特异性一致性,证明R-CHIP能够有效地实现对HPV-16和HPV-18的鉴别诊断。这种集成方案不仅提高了检测的准确性和可靠性,还为资源有限环境下的快速、精准诊断提供了强有力的支持。
最后,为了提升R-CHIP的检测效率并实现HPV病例信息数据的实时收集与模型优化,研究团队进一步开发了基于ResNet-18的深度学习诊断模型。该模型通过智能手机的微成像系统对芯片内的荧光信号进行实时分类,并直接输出针对HPV-16、HPV-18及其混合感染的诊断结果。在对100例临床样本的验证实验中,该系统展现了超过95.0%的准确率。结合便捷的操作方式和先进的数据分析技术,R-CHIP大幅提升了HPV筛查的便利性和普及度。
总体而言,R-CHIP作为技术创新与医疗公平性的结合体,旨在将精准分子诊断技术从实验室推广至社区,从发达国家扩展到发展中国家,实现疾病防控的“最后一公里”。该技术不仅克服了当前多重PCR方法在资源匮乏地区的应用瓶颈,还为全球宫颈癌及其他急慢性传染病的防控提供了智能化解决方案。
论文链接:https://doi.org/10.1002/advs.202414918