
2025年3月26日Science Advances在期刊官网首页以featured image的形式重点报道了raybet官网樊锦轩博士、刘波副教授和赵元弟教授合作完成的研究论文“Programmable engineered bacteria as sustained-releasing antibody factory in situ for enhancing tumor immune checkpoint therapy”,该研究报道了一种作为原位免疫检查点抗体工厂的肿瘤微环境智能响应重编程工程菌,为肿瘤免疫治疗提供了个性化的解决方案。

传统免疫检查点治疗(ICT)依赖T细胞,面临肿瘤微环境复杂、T细胞耗竭等瓶颈,基于巨噬细胞的先天免疫治疗有望成为下一代免疫治疗技术的突破。然而,巨噬细胞免疫治疗的发展受限于“CD47-SIRPα”信号逃逸、系统性治疗引发的溶血风险等问题。当前以单克隆抗体为主的免疫检查点抑制剂(ICIs)具有蛋白类药物的普遍缺陷:体内清除率高、靶向精准性不足、局部浓度难以维持且治疗成本高昂,这些因素阻碍了基于巨噬细胞的免疫检查点治疗发展。
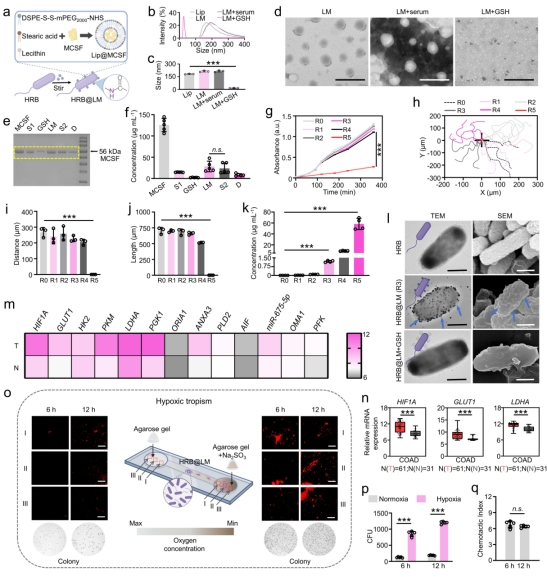
为应对上述挑战,团队通过合成生物学技术,构建了肿瘤乏氧微环境响应型工程菌(HRB)与脂质体(LM)复合的杂化系统HRB@LM:工程菌携带乏氧启动子Pfdh和CD47抗体基因,在肿瘤乏氧微环境中原位合成抗体并外泌;表面修饰的GSH响应型脂质体可释放巨噬细胞集落刺激因子MCSF,促进更多巨噬细胞浸润肿瘤;细菌LPS作为天然佐剂刺激巨噬细胞向肿瘤抑制分型M1极化;同步实现肠道菌群(乳杆菌科/链球菌科等)的显著改善,提升治疗耐受性。
该研究克服传统蛋白药物靶向性差、成本高的局限,时空精准调控:"智能工厂"按需生产抗体,协同激活先天/适应性免疫,并重塑肠道菌群微生态。围绕肿瘤微环境特性和ICT设计的活性“抗体工厂”,为下一代智能化、个性化免疫治疗提供了新范式。
RAYBET雷竞技博士研究生谢晓婷、博士研究生关萌及程凯助理研究员为共同第一作者,樊锦轩博士、刘波副教授和赵元弟教授为共同通讯作者。
该研究得到了国家自然科学基金项目(52103319,62375093,62305121,82373104),中国博士后科学基金资助项目(2023T160247),湖北省重点研发计划项目(2024BCB058),湖北省自然科学基金(2024AFB700)等支持。
论文链接:https://www.science.org/doi/10.1126/sciadv.adt7298